A Química é uma ciência fascinante que estuda a matéria... Mostrar mais
Resumos de Química para o 10º Ano: Principais Conceitos























Átomo
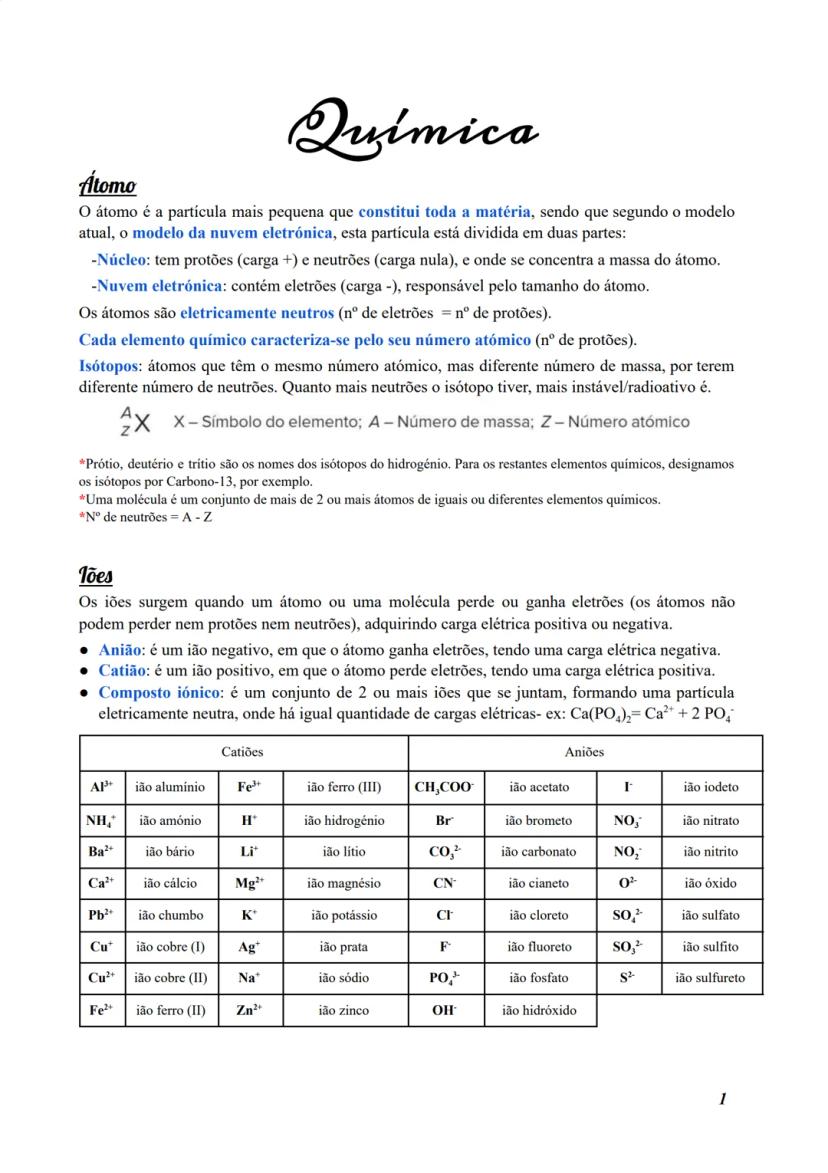
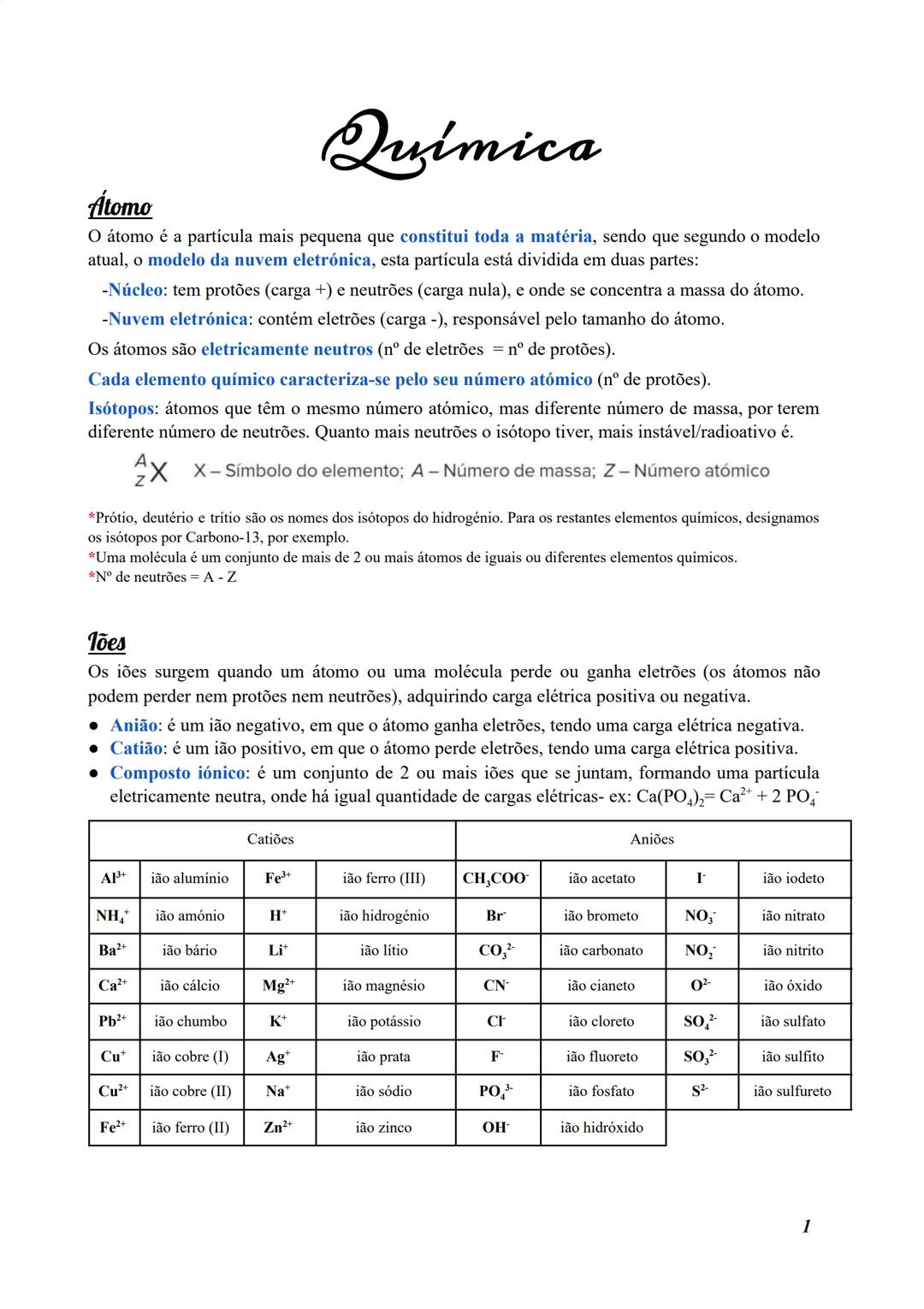
O átomo é a partícula mais pequena que constitui toda a matéria. Segundo o modelo atual (nuvem eletrónica), está dividido em duas partes principais:
- Núcleo: contém protões (carga positiva) e neutrões (carga nula), concentrando a massa do átomo
- Nuvem eletrónica: região onde se encontram os eletrões (carga negativa), responsável pelo tamanho do átomo
Os átomos são eletricamente neutros, pois o número de eletrões é igual ao número de protões. Cada elemento químico é caracterizado pelo seu número atómico (Z), que corresponde ao número de protões.
⚠️ Atenção! Isótopos são átomos do mesmo elemento com diferente número de neutrões. Quanto mais neutrões tiver um isótopo, mais instável/radioativo ele tende a ser.
Para representar um elemento, usamos a notação , onde:
- X é o símbolo do elemento
- A é o número de massa
- Z é o número atómico (protões)
O número de neutrões pode ser calculado por: A - Z = número de neutrões.
Iões
Os iões formam-se quando um átomo ou molécula perde ou ganha eletrões, adquirindo carga elétrica. Existem dois tipos principais:
- Anião: ião negativo, formado quando um átomo ganha eletrões
- Catião: ião positivo, formado quando um átomo perde eletrões
Um composto iónico é o conjunto de dois ou mais iões que formam uma partícula eletricamente neutra. Por exemplo: Ca(PO₄)₂ = Ca²⁺ + 2 PO₄³⁻
Alguns iões importantes incluem:
- Catiões: Al³⁺, NH₄⁺, Ca²⁺, Na⁺, K⁺, Fe²⁺
- Aniões: Cl⁻, F⁻, PO₄³⁻, SO₄²⁻, OH⁻, CO₃²⁻

Massa e Quantidade Química
A massa atómica relativa (Ar) indica quantas vezes a massa de um átomo é maior que a massa padrão . Não tem unidades de medida.
Para elementos com vários isótopos na natureza, calculamos a massa atómica relativa média:
Ar(X) = ÷ 100
A massa molecular relativa (Mr) indica quantas vezes a massa de uma molécula é maior que a massa padrão. Calcula-se somando as massas atómicas relativas de todos os átomos da molécula.
A quantidade química (n) é medida em moles (mol) e corresponde à quantidade de substância que contém 6,022 × 10²³ entidades (Constante de Avogadro, Nₐ).
N = n × Nₐ, onde N é o número de partículas
💡 Uma mole é como uma "dúzia" especial para os químicos - em vez de 12 objetos, contém 6,022 × 10²³ partículas!
A massa molar (M) é a massa de 1 mol de uma substância, expressa em g/mol. Seu valor numérico é igual ao da massa atómica relativa ou molecular relativa:
M = m/n g/mol, onde m é a massa da amostra
A fração molar indica a proporção de uma substância numa mistura:
Xₐ = nₐ/ = nₐ/nTotal
A soma das frações molares de todas as substâncias numa mistura é sempre igual a 1.

Radiação e Luz
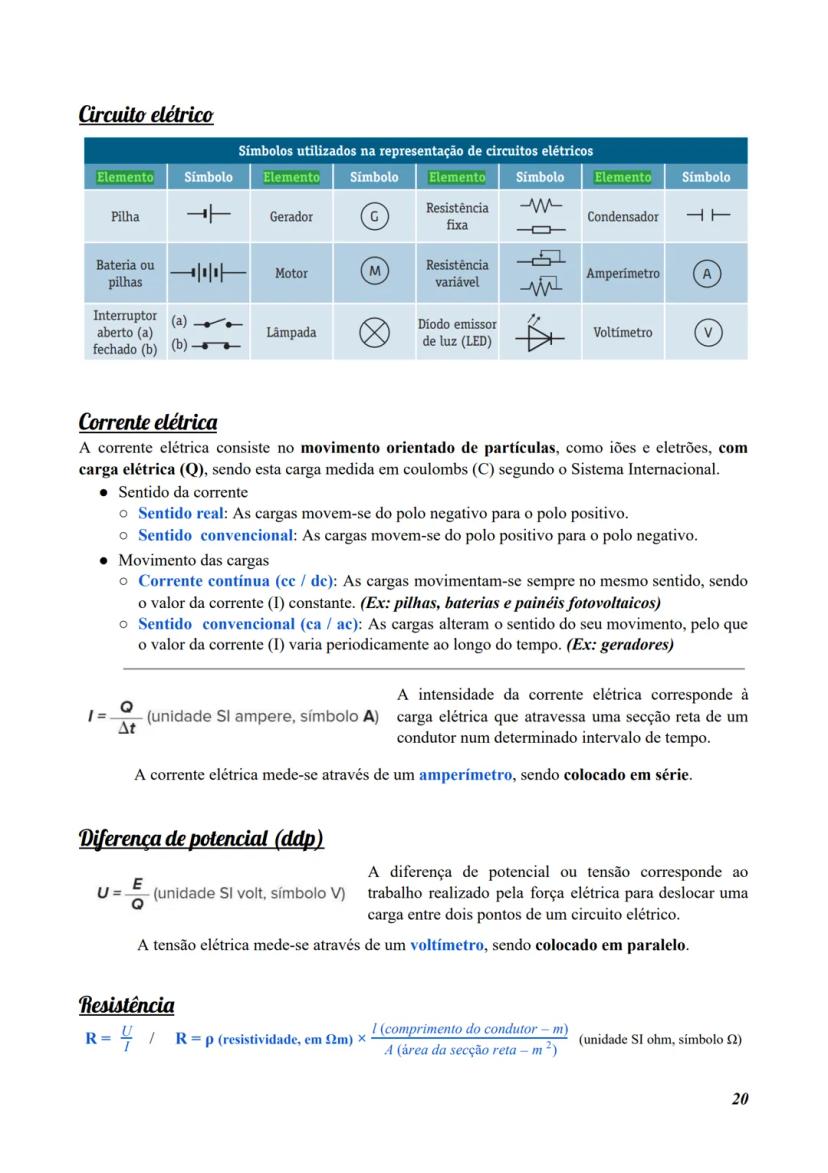
A luz propaga-se pelo espaço através de ondas eletromagnéticas, caracterizadas por três propriedades fundamentais:
- Frequência : número de oscilações por segundo, medida em hertz (Hz)
- Período (T): tempo de uma oscilação completa, medido em segundos (s)
- Comprimento de onda (λ): distância percorrida durante uma oscilação, medida em metros (m)
Estas propriedades relacionam-se através das fórmulas: f = 1/T Hz | T = 1/f s | λ = c/f m
Onde c é a velocidade da luz no vácuo .
A menor porção de luz emitida ou absorvida por um átomo chama-se fotão. A energia do fotão (E) relaciona-se com a frequência da luz:
E = n × h × v ou E = n × h × c/λ
Onde h é a constante de Planck (6,6 × 10⁻³⁴ J·s)
⚠️ No espetro eletromagnético, a energia e a frequência aumentam da esquerda para a direita, enquanto o comprimento de onda diminui.
Os espetros são fundamentais para entender como os átomos interagem com a luz:
- Espetro de emissão contínuo: fundo colorido sem interrupções (ex: lâmpadas incandescentes)
- Espetro de emissão descontínuo: fundo preto com riscas coloridas (ex: lâmpadas fluorescentes)
- Espetro de absorção: fundo colorido com riscas pretas (ex: luz solar)
Segundo o modelo atómico de Bohr, os eletrões movem-se em órbitas circulares bem definidas em volta do núcleo, com energias quantizadas. Quando um eletrão muda de nível de energia, ocorre:
- Excitação: absorção de energia para subir de nível
- Desexcitação: libertação de energia ao descer de nível

Transições Eletrónicas
As riscas que aparecem no espetro atómico agrupam-se em séries espetrais (Lyman, Balmer, Paschen, etc.), cada uma correspondendo a transições para um determinado nível de energia.
Quanto menor for o nível de energia em que o eletrão se encontra, mais negativa é a sua energia. Para um eletrão mudar de nível energético, precisa de absorver ou libertar exatamente a diferença de energia entre os níveis:
ΔE = E₍ₙᵢᵥₑₗ fᵢₙₐₗ₎ - E₍ₙᵢᵥₑₗ ᵢₙᵢcᵢₐₗ₎ Joules (J)
- Se ΔE > 0: há absorção de energia
- Se ΔE < 0: há emissão de energia
💡 As riscas dos espetros de emissão e absorção de uma mesma substância coincidem porque os eletrões tendem a regressar ao estado fundamental após excitação.
A energia de ionização é a energia necessária para remover completamente um eletrão de valência do átomo:
E₍ᵢₒₙᵢzₐçãₒ₎ = E₍∞₎ - E₍ₙᵢᵥₑₗ dₒ ₑₗₑₜᵣãₒ₎
Quando um fotão com energia suficiente atinge um átomo, pode não só ionizar o átomo como dar energia cinética ao eletrão ejetado:
E₍fₒₜãₒ₎ = E₍ᵣₑₘₒçãₒ₎ + E₍cᵢₙéₜᵢcₐ₎
A espetroscopia fotoelétrica é uma técnica usada para determinar as energias dos eletrões, medindo suas energias de remoção. Como átomos de elementos diferentes têm valores distintos de energia dos eletrões, esta técnica permite identificar elementos.
No modelo quântico (modelo da nuvem eletrónica), os eletrões movimentam-se em orbitais—regiões em torno do núcleo onde há maior probabilidade de encontrar eletrões com certa energia. A probabilidade de encontrar um eletrão é maior quanto menor for a distância ao núcleo, devido à atração nuclear.

Configuração Eletrónica
O último nível de energia ocupado por eletrões chama-se nível de valência, e os eletrões neste nível são chamados eletrões de valência. O espaço entre o nível de valência e o primeiro nível é o cerne do átomo, onde encontramos os eletrões do cerne.
Cada nível de energia pode conter no máximo 2n² eletrões (onde n é o número do nível), embora cada nível tenda a estabilizar com 8 eletrões.
A distribuição dos eletrões pelas orbitais atómicas deve obedecer a estas regras:
- Princípio de Exclusão de Pauli: Cada orbital comporta no máximo dois eletrões com spins opostos
- Princípio da Energia Mínima: Os eletrões ocupam primeiro as orbitais de menor energia
- Regra de Hund: Em orbitais com a mesma energia, os eletrões distribuem-se de modo a maximizar o número de eletrões desemparelhados
⚠️ O spin é uma propriedade intrínseca dos eletrões que pode assumir apenas dois estados: spin α (↑) e spin β (↓).
A configuração eletrónica pode ser representada de várias formas:
Forma condensada:
₂₀Ca - 1s² 2s² 2p⁶ 3s² 3p⁶ 4s²
Forma não condensada:
₂₀Ca - 1s² 2s² 2p_x² 2p_y² 2p_z² 3s² 3p_x² 3p_y² 3p_z² 4s²
Simplificada (usando gás nobre mais próximo):
₂₀Ca - [Ar] 4s²
A ordem de preenchimento das orbitais segue esta sequência: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → ...
Também é possível representar átomos no estado excitado, por exemplo:
₆C - 1s² 2s¹ 2p³ (em vez da configuração fundamental 1s² 2s² 2p²)
Partículas com configurações eletrónicas iguais chamam-se partículas isoeletrónicas.

Tabela Periódica
A Tabela Periódica atual resulta da evolução de vários modelos históricos. Em 1829, Döbereiner propôs grupos de três elementos com propriedades semelhantes (tríades). Em 1865, Newlands organizou os elementos em grupos de oito (lei das oitavas). Em 1869, Mendeleev criou a primeira tabela organizada por massa atómica e propriedades químicas, prevendo até elementos desconhecidos. Finalmente, em 1913, Moseley publicou a Tabela Periódica moderna.
A Tabela Periódica organiza os elementos por:
- Ordem crescente do número atómico (Z)
- 18 Grupos (colunas verticais) - elementos no mesmo grupo têm igual número de eletrões de valência
- 7 Períodos (linhas horizontais) - elementos no mesmo período têm igual nível de valência
- 4 Blocos (s, p, d, f) - agrupam elementos com a mesma orbital de valência
💡 Para identificar a posição de um elemento, analisa a sua configuração eletrónica. Por exemplo, se C = 1s² 2s² 2p², então pertence ao grupo 14, período 2 e bloco p.
Os elementos podem ser classificados como:
- Metais (80% dos elementos) - boa condutividade, formam catiões facilmente
- Semimetais (7 elementos) - propriedades intermédias
- Não metais - formam aniões facilmente
As propriedades periódicas seguem padrões devido a três fatores principais:
- Número de níveis de energia: mais níveis = menor atração núcleo-nuvem = maior tamanho
- Carga nuclear: maior carga = maior atração núcleo-nuvem = menor tamanho
- Número de eletrões: mais eletrões = maior repulsão eletrónica = maior tamanho

Propriedades Periódicas
O raio atómico corresponde à distância média entre o núcleo e os eletrões de valência. Ele:
- Aumenta ao descer num grupo (mais níveis de energia)
- Diminui da esquerda para a direita num período (maior carga nuclear)
Situações especiais do raio atómico:
- Catião: menor que o átomo original
- Anião: maior que o átomo original
- Partículas isoeletrónicas: maior raio onde a carga nuclear é menor
A energia de ionização é a energia necessária para remover um eletrão de um átomo no estado fundamental. Ela:
- Diminui ao descer num grupo (eletrões mais afastados do núcleo)
- Aumenta da esquerda para a direita num período (maior carga nuclear)
⚠️ É importante distinguir entre propriedades dos elementos químicos (átomos) e propriedades das substâncias elementares (moléculas formadas por átomos do mesmo elemento).
Algumas famílias importantes da Tabela Periódica:
Metais Alcalinos (grupo 1)
- 1 eletrão de valência facilmente removido
- Formam iões monopositivos (Na⁺, K⁺, etc.)
- Extremamente reativos com água
- Oxidam facilmente
Metais Alcalinoterrosos (grupo 2)
- 2 eletrões de valência facilmente removidos
- Formam iões dipositivos (Ca²⁺, Mg²⁺, etc.)
- Reativos com água
- Oxidam facilmente
Halogéneos (grupo 17)
- 7 eletrões de valência, tendem a ganhar 1
- Formam iões mononegativos (Cl⁻, F⁻, etc.)
- Muito reativos
- Formam sais com facilidade
Gases Nobres (grupo 18)
- Nível de valência completo
- Extremamente estáveis, quase não reagem
- Existem como gases monoatómicos na atmosfera

Ligação entre Átomos
Quando dois átomos se aproximam, existe uma distância ideal onde a energia do sistema é mínima. Neste ponto, forma-se uma ligação química estável.
A energia de ligação (energia liberada quando a ligação se forma) é simétrica à energia de dissociação (energia necessária para quebrar a ligação).
Existem três tipos principais de ligações químicas:
- Ligação Covalente: ocorre entre não metais, que partilham eletrões de valência localizados
- Ligação Iónica: ocorre quando há transferência de eletrões, formando iões que se atraem
- Ligação Metálica: ocorre entre metais, que partilham eletrões de valência deslocalizados
💡 Numa ligação química, os átomos procuram atingir a estabilidade seguindo o Princípio da Energia Mínima: um sistema tende a adquirir o estado de menor energia possível.
As ligações covalentes podem ser:
| Tipo | Descrição | Exemplo | Representação |
|---|---|---|---|
| Simples | Partilha de 1 par de eletrões | H₂ | H-H |
| Dupla | Partilha de 2 pares de eletrões | O₂ | O=O |
| Tripla | Partilha de 3 pares de eletrões | N₂ | N≡N |
Quanto maior a ordem da ligação:
- Maior a energia de ligação
- Menor o comprimento de ligação
- Mais forte a atração entre átomos
Ao formarem ligações covalentes, os átomos seguem a regra do octeto (tendem a ficar rodeados por 8 eletrões de valência). O hidrogénio é exceção, seguindo a regra do dupleto (2 eletrões).
A geometria molecular é o arranjo espacial dos átomos numa molécula, determinado pela teoria da repulsão dos pares eletrónicos de valência.

Geometria Molecular e Hidrocarbonetos
A polaridade de uma molécula depende da distribuição das cargas elétricas. Nas moléculas apolares, a distribuição é simétrica; nas polares, forma-se um polo positivo e um negativo.
Geometrias moleculares comuns:
- Linear: ângulo de 180° (ex: CO₂) - geralmente apolar
- Angular: ângulo de 104,5° (ex: H₂O) - geralmente polar
- Piramidal trigonal: ângulo de 107,5° (ex: NH₃) - geralmente polar
- Triangular plana: ângulo de 120° (ex: BF₃) - geralmente apolar
- Tetraédrica: ângulo de 109,5° (ex: CH₄) - geralmente apolar
⚠️ A geometria molecular determina muitas propriedades físicas e químicas das substâncias, como ponto de ebulição, solubilidade e reatividade.
Os hidrocarbonetos saturados (alcanos) são compostos orgânicos formados apenas por carbono e hidrogénio, unidos por ligações simples. Sua fórmula geral é C₍ₙ₎H₍₂ₙ₊₂₎.
Os principais alcanos são:
- Metano (CH₄)
- Etano (C₂H₆)
- Propano (C₃H₈)
- Butano (C₄H₁₀)
- Pentano (C₅H₁₂)
- Hexano (C₆H₁₄)
- Heptano (C₇H₁₆)
- Octano (C₈H₁₈)
- Nonano (C₉H₂₀)
- Decano (C₁₀H₂₂)
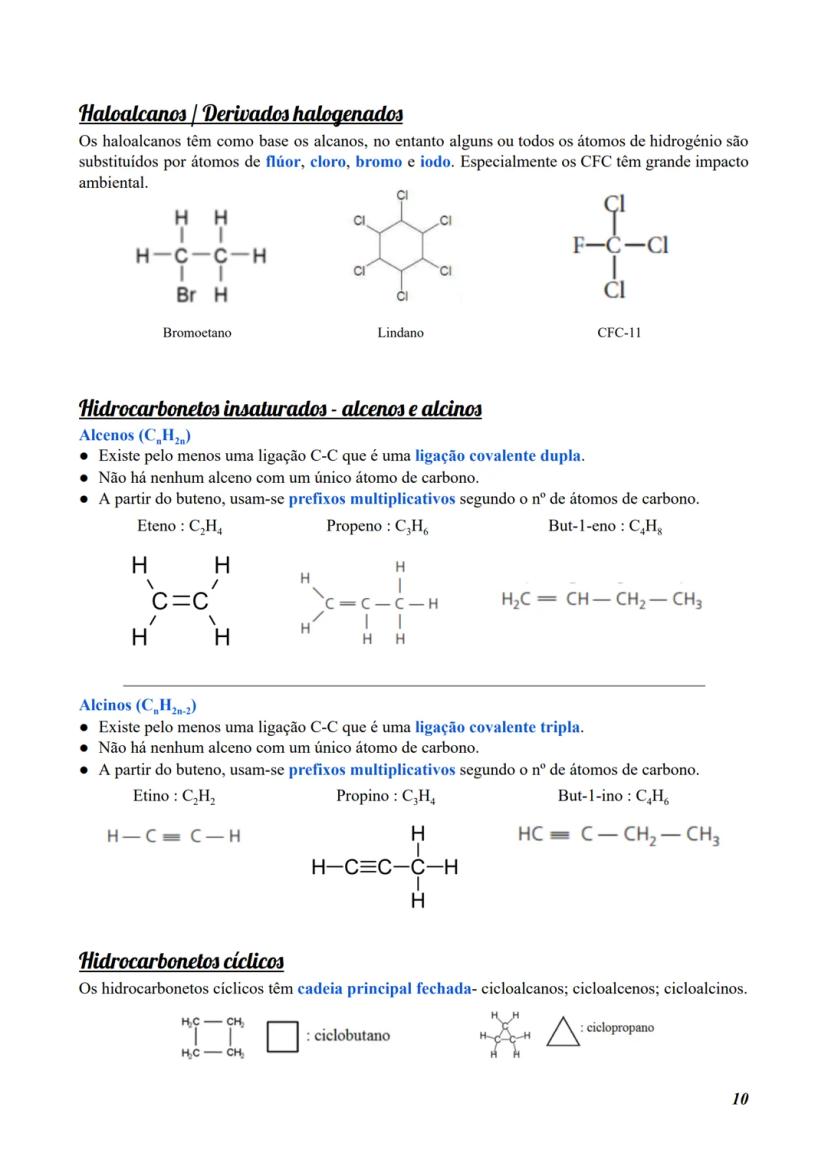
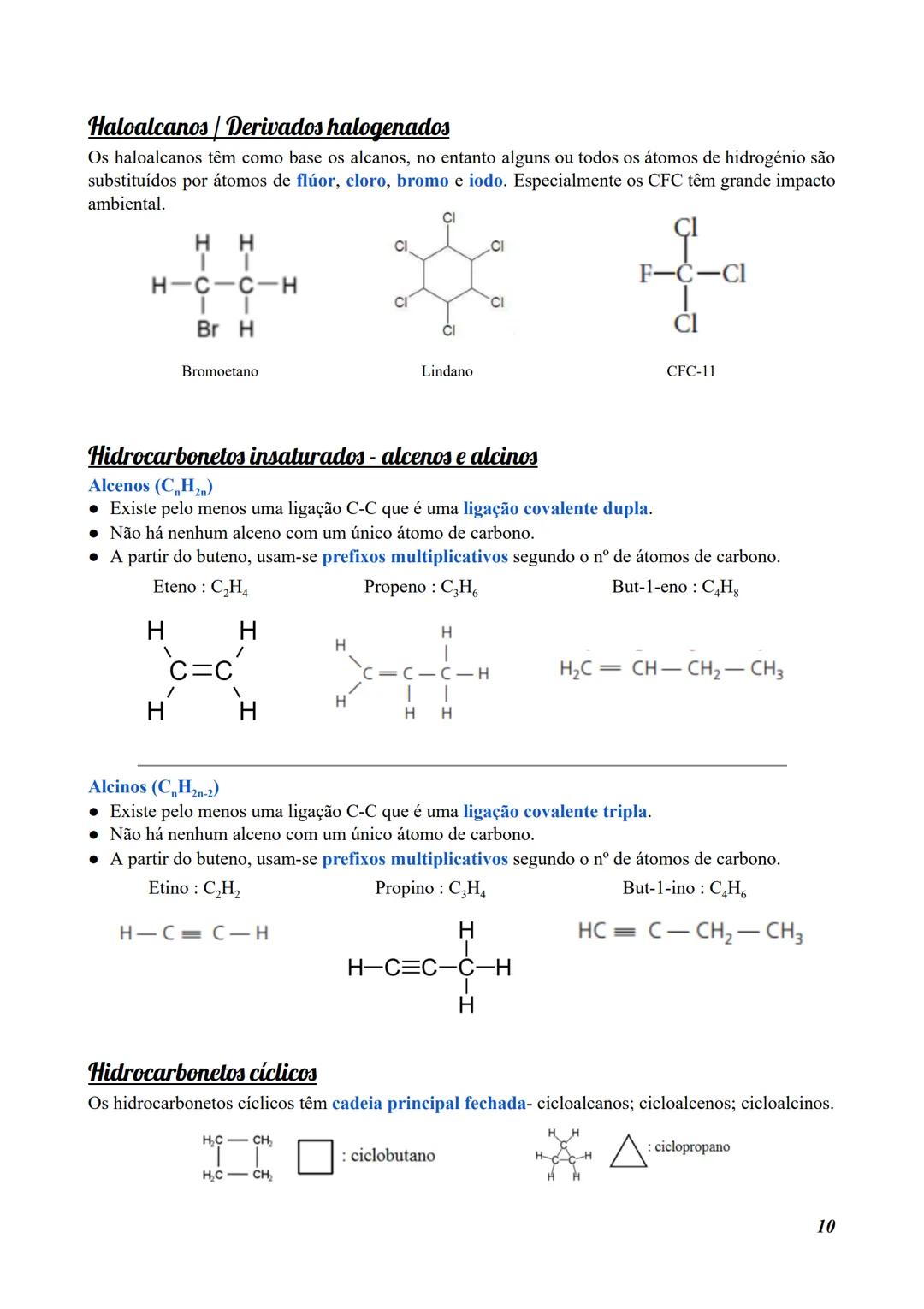
Os haloalcanos (derivados halogenados) são alcanos em que alguns ou todos os átomos de hidrogénio são substituídos por halogéneos (F, Cl, Br, I). Um exemplo são os CFC (clorofluorcarbonetos), que têm impacto ambiental negativo.
Alguns exemplos incluem:
- Bromoetano
- Lindano
- CFC-11
Hidrocarbonetos Insaturados e Cíclicos
Os hidrocarbonetos insaturados contêm ligações duplas ou triplas entre átomos de carbono:
Alcenos (C₍ₙ₎H₍₂ₙ₎)
- Têm pelo menos uma ligação dupla C=C
- Não existem com um único átomo de carbono
- Exemplos:
- Eteno (C₂H₄): H₂C=CH₂
- Propeno (C₃H₆): H₂C=CH-CH₃
- But-1-eno (C₄H₈): H₂C=CH-CH₂-CH₃
Alcinos (C₍ₙ₎H₍₂ₙ₋₂₎)
- Têm pelo menos uma ligação tripla C≡C
- Não existem com um único átomo de carbono
- Exemplos:
- Etino/Acetileno (C₂H₂): HC≡CH
- Propino (C₃H₄): HC≡C-CH₃
- But-1-ino (C₄H₆): HC≡C-CH₂-CH₃
💡 A partir do buteno e do butino, usa-se um número para indicar a posição da ligação dupla ou tripla na cadeia carbonada.
Os hidrocarbonetos cíclicos possuem cadeia principal fechada em anel:
- Cicloalcanos: anéis de carbono com ligações simples (ex: ciclopropano, ciclobutano)
- Cicloalcenos: anéis de carbono com pelo menos uma ligação dupla
- Cicloalcinos: anéis de carbono com pelo menos uma ligação tripla
Estes compostos são fundamentais para a indústria petroquímica, produção de plásticos, medicamentos, combustíveis e muitos outros produtos do nosso quotidiano.















Pensávamos que não ias perguntar...
O que é o Companheiro de Aprendizagem com IA da Knowunity?
O nosso companheiro de aprendizagem com IA foi especificamente criado para as necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos fornecer respostas verdadeiramente significativas e relevantes para os estudantes. Mas não se trata apenas de respostas, o companheiro foca-se mais em guiar os estudantes através dos seus desafios diários de aprendizagem, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização baseada nas habilidades e desenvolvimentos do estudante.
Onde posso fazer o download da app Knowunity?
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Como posso receber o meu pagamento? Quanto posso ganhar?
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
Conteúdos mais populares: Properties of Matter
2Conteúdos mais populares de Química
9Equilíbrio químico
Constante de equilíbrio,quociente da reação, princípio de Le Châtelier, efeito da concentração no equilíbrio
Resumos química 11
Resumos da primeira matéria
Química de 10 ano
Matéria de química do 10 ano, de acordo com as aprendizagens essenciais com base em diversos recursos de modo a ser o mais completo possível. Espero que isto ajude outros tanto quanto me ajudou a mim.
Resumos quimica 10 ano
Resumos quimica
Gases e dispersões
Química 10° ano
gases e dispersoes
resumo quimica 10 ano
Quimica 10 ano
Resumos constituição dos átomos, massa atómica, quantidade de matéria, constante de Avogadro, massa molar, espetro eletromagnético e espetro atómico 10 ano
Química- quantidade de matéria
Quantidade de matéria, massa molecular relativa, massa molar.
química 10 ano
geometria molecular e compostos orgânicos
Conteúdos mais populares
9Resumos Exame Português
Completos
Biologia 10°ano
Resumo completo de biologia de 10°ano
Os Maias
tudo o que necessitas de saber para o teste
Resumos Filosofia 10º ano & 11º ano
Resumos muito completos e explicativos de praticamente toda a matéria da disciplina de Filosofia no ensino secundário em Portugal @mariiarafael
Geologia 11°ano
Resumo completo de Geologia 11ºano
Resumos biologia 10 ano
Resumo completo biologia 10 ano
resumos filosofia 10 e 11 ano
resumos completos de toda a matéria de filosofia de 10 e 11 ano. preparação para exame de filosofia
Resumo dos Maias de Eça de Queiroz
Resumo da obra os Maias de Eça de Queiroz. Naturalismo e realismo, caracterização dos personagens e contexto histórico.
Amor de Perdição
Resumo completo
Não encontra o que procura? Explore outras disciplinas.
Avaliações dos nossos utilizadores. Eles adoraram tudo — e tu também vais adorar.
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.
Resumos de Química para o 10º Ano: Principais Conceitos
A Química é uma ciência fascinante que estuda a matéria e suas transformações. Para entendê-la, precisamos começar pelo básico: o átomo, a menor partícula que constitui toda a matéria. Vamos explorar a estrutura atômica, as ligações químicas e outros conceitos... Mostrar mais

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Átomo
O átomo é a partícula mais pequena que constitui toda a matéria. Segundo o modelo atual (nuvem eletrónica), está dividido em duas partes principais:
- Núcleo: contém protões (carga positiva) e neutrões (carga nula), concentrando a massa do átomo
- Nuvem eletrónica: região onde se encontram os eletrões (carga negativa), responsável pelo tamanho do átomo
Os átomos são eletricamente neutros, pois o número de eletrões é igual ao número de protões. Cada elemento químico é caracterizado pelo seu número atómico (Z), que corresponde ao número de protões.
⚠️ Atenção! Isótopos são átomos do mesmo elemento com diferente número de neutrões. Quanto mais neutrões tiver um isótopo, mais instável/radioativo ele tende a ser.
Para representar um elemento, usamos a notação , onde:
- X é o símbolo do elemento
- A é o número de massa
- Z é o número atómico (protões)
O número de neutrões pode ser calculado por: A - Z = número de neutrões.
Iões
Os iões formam-se quando um átomo ou molécula perde ou ganha eletrões, adquirindo carga elétrica. Existem dois tipos principais:
- Anião: ião negativo, formado quando um átomo ganha eletrões
- Catião: ião positivo, formado quando um átomo perde eletrões
Um composto iónico é o conjunto de dois ou mais iões que formam uma partícula eletricamente neutra. Por exemplo: Ca(PO₄)₂ = Ca²⁺ + 2 PO₄³⁻
Alguns iões importantes incluem:
- Catiões: Al³⁺, NH₄⁺, Ca²⁺, Na⁺, K⁺, Fe²⁺
- Aniões: Cl⁻, F⁻, PO₄³⁻, SO₄²⁻, OH⁻, CO₃²⁻

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Massa e Quantidade Química
A massa atómica relativa (Ar) indica quantas vezes a massa de um átomo é maior que a massa padrão . Não tem unidades de medida.
Para elementos com vários isótopos na natureza, calculamos a massa atómica relativa média:
Ar(X) = ÷ 100
A massa molecular relativa (Mr) indica quantas vezes a massa de uma molécula é maior que a massa padrão. Calcula-se somando as massas atómicas relativas de todos os átomos da molécula.
A quantidade química (n) é medida em moles (mol) e corresponde à quantidade de substância que contém 6,022 × 10²³ entidades (Constante de Avogadro, Nₐ).
N = n × Nₐ, onde N é o número de partículas
💡 Uma mole é como uma "dúzia" especial para os químicos - em vez de 12 objetos, contém 6,022 × 10²³ partículas!
A massa molar (M) é a massa de 1 mol de uma substância, expressa em g/mol. Seu valor numérico é igual ao da massa atómica relativa ou molecular relativa:
M = m/n g/mol, onde m é a massa da amostra
A fração molar indica a proporção de uma substância numa mistura:
Xₐ = nₐ/ = nₐ/nTotal
A soma das frações molares de todas as substâncias numa mistura é sempre igual a 1.

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Radiação e Luz
A luz propaga-se pelo espaço através de ondas eletromagnéticas, caracterizadas por três propriedades fundamentais:
- Frequência : número de oscilações por segundo, medida em hertz (Hz)
- Período (T): tempo de uma oscilação completa, medido em segundos (s)
- Comprimento de onda (λ): distância percorrida durante uma oscilação, medida em metros (m)
Estas propriedades relacionam-se através das fórmulas: f = 1/T Hz | T = 1/f s | λ = c/f m
Onde c é a velocidade da luz no vácuo .
A menor porção de luz emitida ou absorvida por um átomo chama-se fotão. A energia do fotão (E) relaciona-se com a frequência da luz:
E = n × h × v ou E = n × h × c/λ
Onde h é a constante de Planck (6,6 × 10⁻³⁴ J·s)
⚠️ No espetro eletromagnético, a energia e a frequência aumentam da esquerda para a direita, enquanto o comprimento de onda diminui.
Os espetros são fundamentais para entender como os átomos interagem com a luz:
- Espetro de emissão contínuo: fundo colorido sem interrupções (ex: lâmpadas incandescentes)
- Espetro de emissão descontínuo: fundo preto com riscas coloridas (ex: lâmpadas fluorescentes)
- Espetro de absorção: fundo colorido com riscas pretas (ex: luz solar)
Segundo o modelo atómico de Bohr, os eletrões movem-se em órbitas circulares bem definidas em volta do núcleo, com energias quantizadas. Quando um eletrão muda de nível de energia, ocorre:
- Excitação: absorção de energia para subir de nível
- Desexcitação: libertação de energia ao descer de nível

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Transições Eletrónicas
As riscas que aparecem no espetro atómico agrupam-se em séries espetrais (Lyman, Balmer, Paschen, etc.), cada uma correspondendo a transições para um determinado nível de energia.
Quanto menor for o nível de energia em que o eletrão se encontra, mais negativa é a sua energia. Para um eletrão mudar de nível energético, precisa de absorver ou libertar exatamente a diferença de energia entre os níveis:
ΔE = E₍ₙᵢᵥₑₗ fᵢₙₐₗ₎ - E₍ₙᵢᵥₑₗ ᵢₙᵢcᵢₐₗ₎ Joules (J)
- Se ΔE > 0: há absorção de energia
- Se ΔE < 0: há emissão de energia
💡 As riscas dos espetros de emissão e absorção de uma mesma substância coincidem porque os eletrões tendem a regressar ao estado fundamental após excitação.
A energia de ionização é a energia necessária para remover completamente um eletrão de valência do átomo:
E₍ᵢₒₙᵢzₐçãₒ₎ = E₍∞₎ - E₍ₙᵢᵥₑₗ dₒ ₑₗₑₜᵣãₒ₎
Quando um fotão com energia suficiente atinge um átomo, pode não só ionizar o átomo como dar energia cinética ao eletrão ejetado:
E₍fₒₜãₒ₎ = E₍ᵣₑₘₒçãₒ₎ + E₍cᵢₙéₜᵢcₐ₎
A espetroscopia fotoelétrica é uma técnica usada para determinar as energias dos eletrões, medindo suas energias de remoção. Como átomos de elementos diferentes têm valores distintos de energia dos eletrões, esta técnica permite identificar elementos.
No modelo quântico (modelo da nuvem eletrónica), os eletrões movimentam-se em orbitais—regiões em torno do núcleo onde há maior probabilidade de encontrar eletrões com certa energia. A probabilidade de encontrar um eletrão é maior quanto menor for a distância ao núcleo, devido à atração nuclear.

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Configuração Eletrónica
O último nível de energia ocupado por eletrões chama-se nível de valência, e os eletrões neste nível são chamados eletrões de valência. O espaço entre o nível de valência e o primeiro nível é o cerne do átomo, onde encontramos os eletrões do cerne.
Cada nível de energia pode conter no máximo 2n² eletrões (onde n é o número do nível), embora cada nível tenda a estabilizar com 8 eletrões.
A distribuição dos eletrões pelas orbitais atómicas deve obedecer a estas regras:
- Princípio de Exclusão de Pauli: Cada orbital comporta no máximo dois eletrões com spins opostos
- Princípio da Energia Mínima: Os eletrões ocupam primeiro as orbitais de menor energia
- Regra de Hund: Em orbitais com a mesma energia, os eletrões distribuem-se de modo a maximizar o número de eletrões desemparelhados
⚠️ O spin é uma propriedade intrínseca dos eletrões que pode assumir apenas dois estados: spin α (↑) e spin β (↓).
A configuração eletrónica pode ser representada de várias formas:
Forma condensada:
₂₀Ca - 1s² 2s² 2p⁶ 3s² 3p⁶ 4s²
Forma não condensada:
₂₀Ca - 1s² 2s² 2p_x² 2p_y² 2p_z² 3s² 3p_x² 3p_y² 3p_z² 4s²
Simplificada (usando gás nobre mais próximo):
₂₀Ca - [Ar] 4s²
A ordem de preenchimento das orbitais segue esta sequência: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → ...
Também é possível representar átomos no estado excitado, por exemplo:
₆C - 1s² 2s¹ 2p³ (em vez da configuração fundamental 1s² 2s² 2p²)
Partículas com configurações eletrónicas iguais chamam-se partículas isoeletrónicas.

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Tabela Periódica
A Tabela Periódica atual resulta da evolução de vários modelos históricos. Em 1829, Döbereiner propôs grupos de três elementos com propriedades semelhantes (tríades). Em 1865, Newlands organizou os elementos em grupos de oito (lei das oitavas). Em 1869, Mendeleev criou a primeira tabela organizada por massa atómica e propriedades químicas, prevendo até elementos desconhecidos. Finalmente, em 1913, Moseley publicou a Tabela Periódica moderna.
A Tabela Periódica organiza os elementos por:
- Ordem crescente do número atómico (Z)
- 18 Grupos (colunas verticais) - elementos no mesmo grupo têm igual número de eletrões de valência
- 7 Períodos (linhas horizontais) - elementos no mesmo período têm igual nível de valência
- 4 Blocos (s, p, d, f) - agrupam elementos com a mesma orbital de valência
💡 Para identificar a posição de um elemento, analisa a sua configuração eletrónica. Por exemplo, se C = 1s² 2s² 2p², então pertence ao grupo 14, período 2 e bloco p.
Os elementos podem ser classificados como:
- Metais (80% dos elementos) - boa condutividade, formam catiões facilmente
- Semimetais (7 elementos) - propriedades intermédias
- Não metais - formam aniões facilmente
As propriedades periódicas seguem padrões devido a três fatores principais:
- Número de níveis de energia: mais níveis = menor atração núcleo-nuvem = maior tamanho
- Carga nuclear: maior carga = maior atração núcleo-nuvem = menor tamanho
- Número de eletrões: mais eletrões = maior repulsão eletrónica = maior tamanho

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Propriedades Periódicas
O raio atómico corresponde à distância média entre o núcleo e os eletrões de valência. Ele:
- Aumenta ao descer num grupo (mais níveis de energia)
- Diminui da esquerda para a direita num período (maior carga nuclear)
Situações especiais do raio atómico:
- Catião: menor que o átomo original
- Anião: maior que o átomo original
- Partículas isoeletrónicas: maior raio onde a carga nuclear é menor
A energia de ionização é a energia necessária para remover um eletrão de um átomo no estado fundamental. Ela:
- Diminui ao descer num grupo (eletrões mais afastados do núcleo)
- Aumenta da esquerda para a direita num período (maior carga nuclear)
⚠️ É importante distinguir entre propriedades dos elementos químicos (átomos) e propriedades das substâncias elementares (moléculas formadas por átomos do mesmo elemento).
Algumas famílias importantes da Tabela Periódica:
Metais Alcalinos (grupo 1)
- 1 eletrão de valência facilmente removido
- Formam iões monopositivos (Na⁺, K⁺, etc.)
- Extremamente reativos com água
- Oxidam facilmente
Metais Alcalinoterrosos (grupo 2)
- 2 eletrões de valência facilmente removidos
- Formam iões dipositivos (Ca²⁺, Mg²⁺, etc.)
- Reativos com água
- Oxidam facilmente
Halogéneos (grupo 17)
- 7 eletrões de valência, tendem a ganhar 1
- Formam iões mononegativos (Cl⁻, F⁻, etc.)
- Muito reativos
- Formam sais com facilidade
Gases Nobres (grupo 18)
- Nível de valência completo
- Extremamente estáveis, quase não reagem
- Existem como gases monoatómicos na atmosfera

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Ligação entre Átomos
Quando dois átomos se aproximam, existe uma distância ideal onde a energia do sistema é mínima. Neste ponto, forma-se uma ligação química estável.
A energia de ligação (energia liberada quando a ligação se forma) é simétrica à energia de dissociação (energia necessária para quebrar a ligação).
Existem três tipos principais de ligações químicas:
- Ligação Covalente: ocorre entre não metais, que partilham eletrões de valência localizados
- Ligação Iónica: ocorre quando há transferência de eletrões, formando iões que se atraem
- Ligação Metálica: ocorre entre metais, que partilham eletrões de valência deslocalizados
💡 Numa ligação química, os átomos procuram atingir a estabilidade seguindo o Princípio da Energia Mínima: um sistema tende a adquirir o estado de menor energia possível.
As ligações covalentes podem ser:
| Tipo | Descrição | Exemplo | Representação |
|---|---|---|---|
| Simples | Partilha de 1 par de eletrões | H₂ | H-H |
| Dupla | Partilha de 2 pares de eletrões | O₂ | O=O |
| Tripla | Partilha de 3 pares de eletrões | N₂ | N≡N |
Quanto maior a ordem da ligação:
- Maior a energia de ligação
- Menor o comprimento de ligação
- Mais forte a atração entre átomos
Ao formarem ligações covalentes, os átomos seguem a regra do octeto (tendem a ficar rodeados por 8 eletrões de valência). O hidrogénio é exceção, seguindo a regra do dupleto (2 eletrões).
A geometria molecular é o arranjo espacial dos átomos numa molécula, determinado pela teoria da repulsão dos pares eletrónicos de valência.

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Geometria Molecular e Hidrocarbonetos
A polaridade de uma molécula depende da distribuição das cargas elétricas. Nas moléculas apolares, a distribuição é simétrica; nas polares, forma-se um polo positivo e um negativo.
Geometrias moleculares comuns:
- Linear: ângulo de 180° (ex: CO₂) - geralmente apolar
- Angular: ângulo de 104,5° (ex: H₂O) - geralmente polar
- Piramidal trigonal: ângulo de 107,5° (ex: NH₃) - geralmente polar
- Triangular plana: ângulo de 120° (ex: BF₃) - geralmente apolar
- Tetraédrica: ângulo de 109,5° (ex: CH₄) - geralmente apolar
⚠️ A geometria molecular determina muitas propriedades físicas e químicas das substâncias, como ponto de ebulição, solubilidade e reatividade.
Os hidrocarbonetos saturados (alcanos) são compostos orgânicos formados apenas por carbono e hidrogénio, unidos por ligações simples. Sua fórmula geral é C₍ₙ₎H₍₂ₙ₊₂₎.
Os principais alcanos são:
- Metano (CH₄)
- Etano (C₂H₆)
- Propano (C₃H₈)
- Butano (C₄H₁₀)
- Pentano (C₅H₁₂)
- Hexano (C₆H₁₄)
- Heptano (C₇H₁₆)
- Octano (C₈H₁₈)
- Nonano (C₉H₂₀)
- Decano (C₁₀H₂₂)
Os haloalcanos (derivados halogenados) são alcanos em que alguns ou todos os átomos de hidrogénio são substituídos por halogéneos (F, Cl, Br, I). Um exemplo são os CFC (clorofluorcarbonetos), que têm impacto ambiental negativo.
Alguns exemplos incluem:
- Bromoetano
- Lindano
- CFC-11

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Hidrocarbonetos Insaturados e Cíclicos
Os hidrocarbonetos insaturados contêm ligações duplas ou triplas entre átomos de carbono:
Alcenos (C₍ₙ₎H₍₂ₙ₎)
- Têm pelo menos uma ligação dupla C=C
- Não existem com um único átomo de carbono
- Exemplos:
- Eteno (C₂H₄): H₂C=CH₂
- Propeno (C₃H₆): H₂C=CH-CH₃
- But-1-eno (C₄H₈): H₂C=CH-CH₂-CH₃
Alcinos (C₍ₙ₎H₍₂ₙ₋₂₎)
- Têm pelo menos uma ligação tripla C≡C
- Não existem com um único átomo de carbono
- Exemplos:
- Etino/Acetileno (C₂H₂): HC≡CH
- Propino (C₃H₄): HC≡C-CH₃
- But-1-ino (C₄H₆): HC≡C-CH₂-CH₃
💡 A partir do buteno e do butino, usa-se um número para indicar a posição da ligação dupla ou tripla na cadeia carbonada.
Os hidrocarbonetos cíclicos possuem cadeia principal fechada em anel:
- Cicloalcanos: anéis de carbono com ligações simples (ex: ciclopropano, ciclobutano)
- Cicloalcenos: anéis de carbono com pelo menos uma ligação dupla
- Cicloalcinos: anéis de carbono com pelo menos uma ligação tripla
Estes compostos são fundamentais para a indústria petroquímica, produção de plásticos, medicamentos, combustíveis e muitos outros produtos do nosso quotidiano.

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes

Cadastre-se para ver o conteúdo. É grátis!
- Acesso a todos os documentos
- Melhore suas notas
- Junte-se a milhões de estudantes
Pensávamos que não ias perguntar...
O que é o Companheiro de Aprendizagem com IA da Knowunity?
O nosso companheiro de aprendizagem com IA foi especificamente criado para as necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos fornecer respostas verdadeiramente significativas e relevantes para os estudantes. Mas não se trata apenas de respostas, o companheiro foca-se mais em guiar os estudantes através dos seus desafios diários de aprendizagem, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização baseada nas habilidades e desenvolvimentos do estudante.
Onde posso fazer o download da app Knowunity?
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Como posso receber o meu pagamento? Quanto posso ganhar?
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
Conteúdos mais populares: Properties of Matter
2Conteúdos mais populares de Química
9Equilíbrio químico
Constante de equilíbrio,quociente da reação, princípio de Le Châtelier, efeito da concentração no equilíbrio
Resumos química 11
Resumos da primeira matéria
Química de 10 ano
Matéria de química do 10 ano, de acordo com as aprendizagens essenciais com base em diversos recursos de modo a ser o mais completo possível. Espero que isto ajude outros tanto quanto me ajudou a mim.
Resumos quimica 10 ano
Resumos quimica
Gases e dispersões
Química 10° ano
gases e dispersoes
resumo quimica 10 ano
Quimica 10 ano
Resumos constituição dos átomos, massa atómica, quantidade de matéria, constante de Avogadro, massa molar, espetro eletromagnético e espetro atómico 10 ano
Química- quantidade de matéria
Quantidade de matéria, massa molecular relativa, massa molar.
química 10 ano
geometria molecular e compostos orgânicos
Conteúdos mais populares
9Resumos Exame Português
Completos
Biologia 10°ano
Resumo completo de biologia de 10°ano
Os Maias
tudo o que necessitas de saber para o teste
Resumos Filosofia 10º ano & 11º ano
Resumos muito completos e explicativos de praticamente toda a matéria da disciplina de Filosofia no ensino secundário em Portugal @mariiarafael
Geologia 11°ano
Resumo completo de Geologia 11ºano
Resumos biologia 10 ano
Resumo completo biologia 10 ano
resumos filosofia 10 e 11 ano
resumos completos de toda a matéria de filosofia de 10 e 11 ano. preparação para exame de filosofia
Resumo dos Maias de Eça de Queiroz
Resumo da obra os Maias de Eça de Queiroz. Naturalismo e realismo, caracterização dos personagens e contexto histórico.
Amor de Perdição
Resumo completo
Não encontra o que procura? Explore outras disciplinas.
Avaliações dos nossos utilizadores. Eles adoraram tudo — e tu também vais adorar.
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.