O modelo de Bohr explica como os eletrões se movem... Mostrar mais
Cadastre-se para ver o conteúdoÉ grátis!
Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Knowunity AI
Disciplinas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos os tópicos
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos os tópicos
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos os tópicos
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos os tópicos
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos os tópicos
490
•
Atualizado Apr 12, 2026
•
Francisca Oliveira
@francisca_4pnmv
O modelo de Bohr explica como os eletrões se movem... Mostrar mais






No modelo de Bohr, os eletrões movem-se em órbitas circulares ao redor do núcleo. Quanto maior o raio da órbita, maior a energia do eletrão, pois a energia resulta da interação com o núcleo. A energia de um eletrão num nível m é dada pela fórmula Em = -2,18×10^-18 J/m².
No átomo de hidrogénio, os níveis de energia são identificados por números . O nível m=1 corresponde ao estado fundamental (menor energia), enquanto m=2, m=3, etc., são estados excitados de energia sucessivamente maiores. Quando o eletrão atinge m=∞, o átomo ioniza-se.
Quando excitados, os eletrões libertam energia ao regressar a níveis de menor energia. Esta libertação manifesta-se pela emissão de radiação com frequência específica, produzindo riscas características no espetro atómico de emissão.
💡 Pensa no átomo como uma escada: o eletrão só pode estar em degraus específicos (níveis) e, ao "descer" de um degrau para outro, liberta energia em forma de luz!
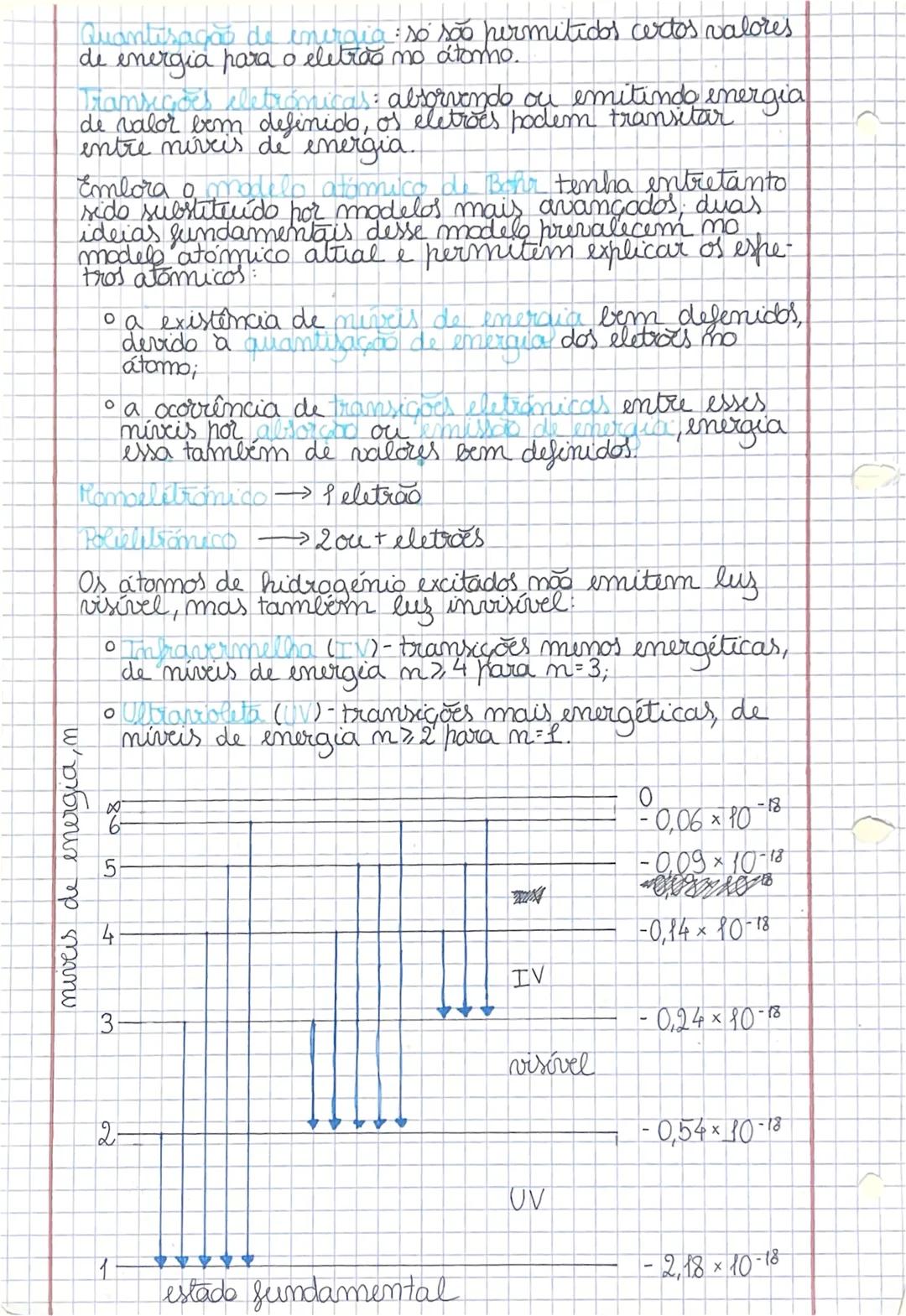
Duas ideias fundamentais do modelo de Bohr ainda prevalecem nos modelos atómicos atuais: a quantização de energia (só são permitidos certos valores de energia para os eletrões) e as transições eletrónicas (os eletrões podem mudar de nível absorvendo ou emitindo energia de valor bem definido).
Os átomos de hidrogénio excitados emitem não só luz visível, mas também luz invisível! As transições menos energéticas produzem radiação infravermelha (IV), enquanto as transições mais energéticas produzem radiação ultravioleta (UV).
Cada transição corresponde a uma diferença de energia específica. Os níveis tornam-se cada vez mais próximos à medida que aumentamos o número do nível, o que explica os diferentes tipos de radiação emitida.
⚠️ Lembra-te: só podemos ver uma pequena parte do espetro eletromagnético! As transições eletrónicas podem produzir radiação em todo o espetro, não apenas luz visível.

A energia dos eletrões nos átomos depende de atrações e repulsões . Cada elemento químico possui um conjunto único de níveis de energia, fazendo com que os espetros atómicos funcionem como "impressões digitais" dos elementos.
Nos átomos, os eletrões de valência (que ocupam o último nível de energia) são os mais fáceis de remover, pois estão mais afastados do núcleo e sofrem menor atração nuclear. Estes eletrões têm menor energia de remoção comparados aos eletrões mais internos.
Por outro lado, os eletrões do nível de energia mais interior estão, em média, mais próximos do núcleo. Isso significa que estão sujeitos a maior atração nuclear, tornando-os mais difíceis de remover e, consequentemente, possuem maior energia de remoção.
🔍 Podes pensar nos eletrões de valência como os últimos membros a juntar-se a uma família - são os primeiros a sair quando há problemas (como quando se aplica energia)!

Para qualquer átomo, a energia do eletrão no nível infinito (E∞) é considerada nula, e o valor absoluto da energia do eletrão no átomo (Em) equivale à energia de remoção.
Os níveis de energia dos átomos dividem-se em subníveis. O menor subnível de cada nível é sempre designado por s. Eletrões no nível n=1 ocupam apenas o subnível 1s. No nível n=2, aparecem os subníveis 2s e 2p. Para níveis n≥3, surgem também subníveis d (como 3d, 4d).
Esta organização em subníveis explica as propriedades químicas dos elementos e seus comportamentos nas ligações. A forma como os eletrões se distribuem nestes subníveis determina características fundamentais dos átomos.
Os espetros fotoeletrónicos obtidos por espetroscopia fotoelétrica registam os valores das energias de remoção, sendo diferentes e característicos para cada elemento químico.
📊 Imagina os subníveis como apartamentos dentro de um mesmo andar: mesmo estando no mesmo nível (andar), alguns apartamentos (subníveis) estão mais próximos ou mais distantes do elevador central (núcleo)!

Num espetro fotoeletrónico, os níveis de energia aparecem separados uns dos outros por uma dupla barra na escala das energias de remoção. O número de picos presentes em cada nível corresponde exatamente ao número de subníveis.
A altura relativa dos picos relaciona-se com o número de eletrões em cada subnível - é proporcional à quantidade de eletrões presentes. Assim, picos da mesma altura correspondem a subníveis com igual número de eletrões.
As energias dos subníveis dentro do mesmo nível principal são relativamente próximas. Por exemplo, os subníveis 2s e 2p têm energias próximas por pertencerem ao nível n=2, mas são muito maiores que a energia do nível n=1. Esta organização energética permite-nos entender a distribuição eletrónica e prever propriedades químicas.
🔬 Os espetros fotoeletrónicos são como uma "radiografia energética" do átomo, revelando sua estrutura eletrónica interna de forma detalhada!
O nosso companheiro de aprendizagem com IA foi especificamente criado para as necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos fornecer respostas verdadeiramente significativas e relevantes para os estudantes. Mas não se trata apenas de respostas, o companheiro foca-se mais em guiar os estudantes através dos seus desafios diários de aprendizagem, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização baseada nas habilidades e desenvolvimentos do estudante.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
App Store
Google Play
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
João S
utilizador iOS
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Sara C.
utilizadora Android
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.
Ana
utilizadora iOS
Eu costumava ter dificuldade para completar os meus trabalhos a tempo até descobrir a Knowunity, que não só facilita o upload do meu próprio conteúdo, mas também oferece ótimos resumos que tornam o meu trabalho mais rápido e eficiente.
Tomás R
utilizador iOS
Sempre foi um desafio encontrar todas as informações importantes para os meus trabalhos – desde que comecei a usar a Knowunity, posso simplesmente fazer upload do meu conteúdo e aproveitar os resumos dos outros, o que me ajuda muito com a organização.
Luísa M
utilizadora Android
Eu frequentemente sentia que não tinha uma visão geral suficiente ao estudar, mas desde que comecei a usar o Knowunity, isso não acontece mais – faço upload do meu conteúdo e encontro sempre resumos úteis na plataforma, o que torna meu aprendizado muito mais fácil.
David F
utilizador iOS
O app é simplesmente incrível! Só preciso digitar o tema na barra de pesquisa e recebo a resposta super rápido. Não preciso assistir 10 vídeos no YouTube para entender algo, então economizo meu tempo. Super recomendo!
Marco O
utilizador Android
Na escola eu era péssimo em matemática, mas graças ao app, estou me saindo melhor agora. Sou muito grato por vocês terem criado o app.
André B
utilizador Android
Costumava ser muito difícil reunir todas as informações para minhas apresentações. Mas desde que comecei a usar o Knowunity, só preciso de carregar os meus apontamentos e encontrar resumos incríveis de outros - isso torna meu estudo muito mais eficiente!
Júlia S
utilizadora Android
Estava constantemente stressado com todo o material de estudo, mas desde que comecei a usar a Knowunity, carrego as minhas coisas e vejo os resumos dos outros - isto ajuda-me a gerir tudo melhor e é muito menos stressante.
Marco B
utilizador iOS
OS QUESTIONÁRIOS E CARTÕES DE ESTUDO SÃO TÃO ÚTEIS E ADORO A IA DA Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! AJUDOU-ME ATÉ COM OS MEUS PROBLEMAS DE RÍMEL!! ASSIM COMO COM AS MINHAS CADEIRAS A SÉRIO! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
utilizadora Android
Eu costumava passar horas no Google à procura de materiais escolares, mas agora só carrego as minhas coisas na Knowunity e vejo os resumos dos outros - sinto-me muito mais confiante quando me preparo para testes.
Paulo T
utilizador iOS
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
João S
utilizador iOS
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Sara C.
utilizadora Android
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.
Ana
utilizadora iOS
Eu costumava ter dificuldade para completar os meus trabalhos a tempo até descobrir a Knowunity, que não só facilita o upload do meu próprio conteúdo, mas também oferece ótimos resumos que tornam o meu trabalho mais rápido e eficiente.
Tomás R
utilizador iOS
Sempre foi um desafio encontrar todas as informações importantes para os meus trabalhos – desde que comecei a usar a Knowunity, posso simplesmente fazer upload do meu conteúdo e aproveitar os resumos dos outros, o que me ajuda muito com a organização.
Luísa M
utilizadora Android
Eu frequentemente sentia que não tinha uma visão geral suficiente ao estudar, mas desde que comecei a usar o Knowunity, isso não acontece mais – faço upload do meu conteúdo e encontro sempre resumos úteis na plataforma, o que torna meu aprendizado muito mais fácil.
David F
utilizador iOS
O app é simplesmente incrível! Só preciso digitar o tema na barra de pesquisa e recebo a resposta super rápido. Não preciso assistir 10 vídeos no YouTube para entender algo, então economizo meu tempo. Super recomendo!
Marco O
utilizador Android
Na escola eu era péssimo em matemática, mas graças ao app, estou me saindo melhor agora. Sou muito grato por vocês terem criado o app.
André B
utilizador Android
Costumava ser muito difícil reunir todas as informações para minhas apresentações. Mas desde que comecei a usar o Knowunity, só preciso de carregar os meus apontamentos e encontrar resumos incríveis de outros - isso torna meu estudo muito mais eficiente!
Júlia S
utilizadora Android
Estava constantemente stressado com todo o material de estudo, mas desde que comecei a usar a Knowunity, carrego as minhas coisas e vejo os resumos dos outros - isto ajuda-me a gerir tudo melhor e é muito menos stressante.
Marco B
utilizador iOS
OS QUESTIONÁRIOS E CARTÕES DE ESTUDO SÃO TÃO ÚTEIS E ADORO A IA DA Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! AJUDOU-ME ATÉ COM OS MEUS PROBLEMAS DE RÍMEL!! ASSIM COMO COM AS MINHAS CADEIRAS A SÉRIO! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
utilizadora Android
Eu costumava passar horas no Google à procura de materiais escolares, mas agora só carrego as minhas coisas na Knowunity e vejo os resumos dos outros - sinto-me muito mais confiante quando me preparo para testes.
Paulo T
utilizador iOS
Francisca Oliveira
@francisca_4pnmv
O modelo de Bohr explica como os eletrões se movem ao redor do núcleo atómico em órbitas de raios definidos. Este modelo introduziu conceitos fundamentais como a quantização de energia e as transições eletrónicas, que são essenciais para compreender o... Mostrar mais

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
No modelo de Bohr, os eletrões movem-se em órbitas circulares ao redor do núcleo. Quanto maior o raio da órbita, maior a energia do eletrão, pois a energia resulta da interação com o núcleo. A energia de um eletrão num nível m é dada pela fórmula Em = -2,18×10^-18 J/m².
No átomo de hidrogénio, os níveis de energia são identificados por números . O nível m=1 corresponde ao estado fundamental (menor energia), enquanto m=2, m=3, etc., são estados excitados de energia sucessivamente maiores. Quando o eletrão atinge m=∞, o átomo ioniza-se.
Quando excitados, os eletrões libertam energia ao regressar a níveis de menor energia. Esta libertação manifesta-se pela emissão de radiação com frequência específica, produzindo riscas características no espetro atómico de emissão.
💡 Pensa no átomo como uma escada: o eletrão só pode estar em degraus específicos (níveis) e, ao "descer" de um degrau para outro, liberta energia em forma de luz!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Duas ideias fundamentais do modelo de Bohr ainda prevalecem nos modelos atómicos atuais: a quantização de energia (só são permitidos certos valores de energia para os eletrões) e as transições eletrónicas (os eletrões podem mudar de nível absorvendo ou emitindo energia de valor bem definido).
Os átomos de hidrogénio excitados emitem não só luz visível, mas também luz invisível! As transições menos energéticas produzem radiação infravermelha (IV), enquanto as transições mais energéticas produzem radiação ultravioleta (UV).
Cada transição corresponde a uma diferença de energia específica. Os níveis tornam-se cada vez mais próximos à medida que aumentamos o número do nível, o que explica os diferentes tipos de radiação emitida.
⚠️ Lembra-te: só podemos ver uma pequena parte do espetro eletromagnético! As transições eletrónicas podem produzir radiação em todo o espetro, não apenas luz visível.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A energia dos eletrões nos átomos depende de atrações e repulsões . Cada elemento químico possui um conjunto único de níveis de energia, fazendo com que os espetros atómicos funcionem como "impressões digitais" dos elementos.
Nos átomos, os eletrões de valência (que ocupam o último nível de energia) são os mais fáceis de remover, pois estão mais afastados do núcleo e sofrem menor atração nuclear. Estes eletrões têm menor energia de remoção comparados aos eletrões mais internos.
Por outro lado, os eletrões do nível de energia mais interior estão, em média, mais próximos do núcleo. Isso significa que estão sujeitos a maior atração nuclear, tornando-os mais difíceis de remover e, consequentemente, possuem maior energia de remoção.
🔍 Podes pensar nos eletrões de valência como os últimos membros a juntar-se a uma família - são os primeiros a sair quando há problemas (como quando se aplica energia)!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Para qualquer átomo, a energia do eletrão no nível infinito (E∞) é considerada nula, e o valor absoluto da energia do eletrão no átomo (Em) equivale à energia de remoção.
Os níveis de energia dos átomos dividem-se em subníveis. O menor subnível de cada nível é sempre designado por s. Eletrões no nível n=1 ocupam apenas o subnível 1s. No nível n=2, aparecem os subníveis 2s e 2p. Para níveis n≥3, surgem também subníveis d (como 3d, 4d).
Esta organização em subníveis explica as propriedades químicas dos elementos e seus comportamentos nas ligações. A forma como os eletrões se distribuem nestes subníveis determina características fundamentais dos átomos.
Os espetros fotoeletrónicos obtidos por espetroscopia fotoelétrica registam os valores das energias de remoção, sendo diferentes e característicos para cada elemento químico.
📊 Imagina os subníveis como apartamentos dentro de um mesmo andar: mesmo estando no mesmo nível (andar), alguns apartamentos (subníveis) estão mais próximos ou mais distantes do elevador central (núcleo)!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Num espetro fotoeletrónico, os níveis de energia aparecem separados uns dos outros por uma dupla barra na escala das energias de remoção. O número de picos presentes em cada nível corresponde exatamente ao número de subníveis.
A altura relativa dos picos relaciona-se com o número de eletrões em cada subnível - é proporcional à quantidade de eletrões presentes. Assim, picos da mesma altura correspondem a subníveis com igual número de eletrões.
As energias dos subníveis dentro do mesmo nível principal são relativamente próximas. Por exemplo, os subníveis 2s e 2p têm energias próximas por pertencerem ao nível n=2, mas são muito maiores que a energia do nível n=1. Esta organização energética permite-nos entender a distribuição eletrónica e prever propriedades químicas.
🔬 Os espetros fotoeletrónicos são como uma "radiografia energética" do átomo, revelando sua estrutura eletrónica interna de forma detalhada!
O nosso companheiro de aprendizagem com IA foi especificamente criado para as necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos fornecer respostas verdadeiramente significativas e relevantes para os estudantes. Mas não se trata apenas de respostas, o companheiro foca-se mais em guiar os estudantes através dos seus desafios diários de aprendizagem, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização baseada nas habilidades e desenvolvimentos do estudante.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
13
Ferramentas Inteligentes NOVO
Transforma estes apontamentos em: ✓ 50+ Questões de Prática ✓ Cartões de Estudo Interactivos ✓ Exame Simulado Completo ✓ Esquemas de Ensaio
App Store
Google Play
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
João S
utilizador iOS
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Sara C.
utilizadora Android
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.
Ana
utilizadora iOS
Eu costumava ter dificuldade para completar os meus trabalhos a tempo até descobrir a Knowunity, que não só facilita o upload do meu próprio conteúdo, mas também oferece ótimos resumos que tornam o meu trabalho mais rápido e eficiente.
Tomás R
utilizador iOS
Sempre foi um desafio encontrar todas as informações importantes para os meus trabalhos – desde que comecei a usar a Knowunity, posso simplesmente fazer upload do meu conteúdo e aproveitar os resumos dos outros, o que me ajuda muito com a organização.
Luísa M
utilizadora Android
Eu frequentemente sentia que não tinha uma visão geral suficiente ao estudar, mas desde que comecei a usar o Knowunity, isso não acontece mais – faço upload do meu conteúdo e encontro sempre resumos úteis na plataforma, o que torna meu aprendizado muito mais fácil.
David F
utilizador iOS
O app é simplesmente incrível! Só preciso digitar o tema na barra de pesquisa e recebo a resposta super rápido. Não preciso assistir 10 vídeos no YouTube para entender algo, então economizo meu tempo. Super recomendo!
Marco O
utilizador Android
Na escola eu era péssimo em matemática, mas graças ao app, estou me saindo melhor agora. Sou muito grato por vocês terem criado o app.
André B
utilizador Android
Costumava ser muito difícil reunir todas as informações para minhas apresentações. Mas desde que comecei a usar o Knowunity, só preciso de carregar os meus apontamentos e encontrar resumos incríveis de outros - isso torna meu estudo muito mais eficiente!
Júlia S
utilizadora Android
Estava constantemente stressado com todo o material de estudo, mas desde que comecei a usar a Knowunity, carrego as minhas coisas e vejo os resumos dos outros - isto ajuda-me a gerir tudo melhor e é muito menos stressante.
Marco B
utilizador iOS
OS QUESTIONÁRIOS E CARTÕES DE ESTUDO SÃO TÃO ÚTEIS E ADORO A IA DA Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! AJUDOU-ME ATÉ COM OS MEUS PROBLEMAS DE RÍMEL!! ASSIM COMO COM AS MINHAS CADEIRAS A SÉRIO! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
utilizadora Android
Eu costumava passar horas no Google à procura de materiais escolares, mas agora só carrego as minhas coisas na Knowunity e vejo os resumos dos outros - sinto-me muito mais confiante quando me preparo para testes.
Paulo T
utilizador iOS
A App é muito fácil de usar e está nem organizada. Encontrei tudo o que estava à procura até agora e consegui aprender muito com as apresentações! Vou usar a app para um trabalho escolar! E claro que também me ajuda muito como inspiração.
João S
utilizador iOS
Esta app é realmente incrível. Há tantas anotações de estudo e ajuda [...]. A minha disciplina problemática é Francês, por exemplo, e a app tem muitas opções de ajuda. Graças a esta app, melhorei o meu Francês. Eu recomendo a qualquer pessoa.
Sara C.
utilizadora Android
Uau, estou realmente impressionado. Acabei de experimentar o app porque o vi anunciado muitas vezes e fiquei absolutamente surpreso. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece tantas coisas, como exercícios e folhas de fatos, que têm sido MUITO úteis para mim pessoalmente.
Ana
utilizadora iOS
Eu costumava ter dificuldade para completar os meus trabalhos a tempo até descobrir a Knowunity, que não só facilita o upload do meu próprio conteúdo, mas também oferece ótimos resumos que tornam o meu trabalho mais rápido e eficiente.
Tomás R
utilizador iOS
Sempre foi um desafio encontrar todas as informações importantes para os meus trabalhos – desde que comecei a usar a Knowunity, posso simplesmente fazer upload do meu conteúdo e aproveitar os resumos dos outros, o que me ajuda muito com a organização.
Luísa M
utilizadora Android
Eu frequentemente sentia que não tinha uma visão geral suficiente ao estudar, mas desde que comecei a usar o Knowunity, isso não acontece mais – faço upload do meu conteúdo e encontro sempre resumos úteis na plataforma, o que torna meu aprendizado muito mais fácil.
David F
utilizador iOS
O app é simplesmente incrível! Só preciso digitar o tema na barra de pesquisa e recebo a resposta super rápido. Não preciso assistir 10 vídeos no YouTube para entender algo, então economizo meu tempo. Super recomendo!
Marco O
utilizador Android
Na escola eu era péssimo em matemática, mas graças ao app, estou me saindo melhor agora. Sou muito grato por vocês terem criado o app.
André B
utilizador Android
Costumava ser muito difícil reunir todas as informações para minhas apresentações. Mas desde que comecei a usar o Knowunity, só preciso de carregar os meus apontamentos e encontrar resumos incríveis de outros - isso torna meu estudo muito mais eficiente!
Júlia S
utilizadora Android
Estava constantemente stressado com todo o material de estudo, mas desde que comecei a usar a Knowunity, carrego as minhas coisas e vejo os resumos dos outros - isto ajuda-me a gerir tudo melhor e é muito menos stressante.
Marco B
utilizador iOS
OS QUESTIONÁRIOS E CARTÕES DE ESTUDO SÃO TÃO ÚTEIS E ADORO A IA DA Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! AJUDOU-ME ATÉ COM OS MEUS PROBLEMAS DE RÍMEL!! ASSIM COMO COM AS MINHAS CADEIRAS A SÉRIO! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
utilizadora Android
Eu costumava passar horas no Google à procura de materiais escolares, mas agora só carrego as minhas coisas na Knowunity e vejo os resumos dos outros - sinto-me muito mais confiante quando me preparo para testes.
Paulo T
utilizador iOS